ПСИХУШКА ЗА ПОБЕГ ИЗ ДЕТДОМА
Две недели назад в Гражданскую комиссию по правам человека поступило очередное сообщение по поводу того, что 15-летнего подростка поместили из обычного детского дома в психиатриче..
| Мой путь в немецкую клинику
Немецкая медицина является для многих врачей одним из эталонов качества, надежности и мастерства. Это и неудивительно - мне, как хирургу, в своей повседневной клинической деятельно..
| Как сдавать PLAB экзамены
лицензии на работу врачом в Великобритании. Однако ему должна предшествовать успешная (с проходным баллом 7) сдача теста по английскому языку (IELTs)...
| Каким быть ногтям медицинского работника
Всемирная организация здравоохранения (ВОЗ) обращает внимание на то, что искусственные акриловые ногти способствуют сохранению контаминации рук после использования мыла или содержа..
| Охота на фармацевтов и врачей
Две трети судебных юристов США, зарабатывающих на процентах от отсуженных компенсаций пострадавшим, специализируются на "медицинских" процессах - исках к производителям лекарств и..
| Клонирован мочевой пузырь
Клонирование человека - дилемма. Клонирование отдельных органов - мечта. Возможность менять старые, отработавшие, больные органы на новые будоражит умы и врачей, и пациентов. Актуа..
| Наш мир в возрасте 84 лет 14 апреля 2003 года покинула Любовь Трофимовна Малая, Герой Украины, Герой Социалистического Труда, кавалер ордена Трудового Красного Знамени; орденоносец..
| Клонирование: прошлое, настоящее, будущее
клонирование клетки животных клонирования клеток клонирование развития эмбрионов генов ядра переноса institute году было ядерного ядер которых человека клонов генетически эмбриона однако время соматической помощьюклонирование овца Долли прогрессирующее заболевание легких клонирования клетки клоны человек воспроизведение живого объекта деления эмбриона метод ядерного переноса замещение ядра клетки реконструированный эмбрион клонирование амфибий мыши кролики пересадка ядер бластомеров имплантация трансплантированные пронуклеусы зигот гипертрофированная плацента
гидроаллантоис плацентома клонированные организмы сускоренное старение фермент теломераза генетически модифицированные поросята замедленный иммунный ответ терапевтическое клонирование стволовые клетки клонирование человека репродуктивное клонирование
Клонирование: прошлое, настоящее, будущее
В феврале 2003 года сотрудники Roslin Institute (Шотландия) сообщили, что им пришлось усыпить первую клонированную шестилетнюю овцу Долли после того, как ветеринары подтвердили наличие у нее прогрессирующего заболевания легких.
Долли появилась на свет в результате клонирования клетки взрослой овцы в 1996 году, которое провела группа ученых под руководством профессора Ian Wilmut. Рождение овцы стало одним из важнейших научных достижений 1990-х годов, но при этом вызвало новые споры в области этики клонирования, особенно в вопросах клонирования человека.
В январе 2002 года у Долли развился артрит, заболевание, встречающееся обычно у старых животных. Не было ясно, связан ли артрит с клонированием, но ученые еще в 1999 году после исследования генома овцы предположили, что ее организм склонен к преждевременному старению. Опасения подтвердились, когда у Долли было выявлено заболевание легких, характерное для особей старшего возраста.
Периодические издания запестрили заголовками, то предрекающими конец эры клонирования, то сообщающими о новых достижениях технологии, вплоть до рождения клонов человека.
Можно с уверенностью сказать, что из всех тем, имеющих отношение к медицине, темы клонирования удерживают первое место по количеству сенсационных заявлений, домыслов, заблуждений и дезинформации.
Что такое клонирование
Клонирование - это воспроизведение живого объекта в некотором количестве копий, обладающих идентичной наследственной информацией, то есть несущих одинаковый набор генов.
По мнению специалистов Roslin Institute, клонированием можно назвать следующие процессы:
- Появление генетически идентичных индивидуумов, полученных от одного родителя с помощью бесполого воспроизведения. Подобное явление свойственно многим растениям, образующим луковицы или клубни.
- Образование генетически идентичных клеток, появившихся в результате митотического деления одной оригинальной клетки, которая создает новый набор хромосом и делится на две дочерние. Такое обновление клеток свойственно различным тканям организма.
- Получение генетически идентичных молекул ДНК из нуклеиновой кислоты бактерии или вируса с использованием методов молекулярной биологии. Этот процесс зачастую называют молекулярным или ДНК-клонированием.
- Создание генетически идентичных организмов путем "деления эмбриона". Нередко у ценных пород
крупного рогатого скота производят искусственное деление эмбриона, пересаживая отдельные клетки из четырех- и восьмиклеточных эмбрионов суррогатным матерям.
- Самое последнее достижение - создание генетически идентичных индивидуумов с использованием принципиально новой технологии которая получила название "метод ядерного переноса" или "замещение ядра клетки".
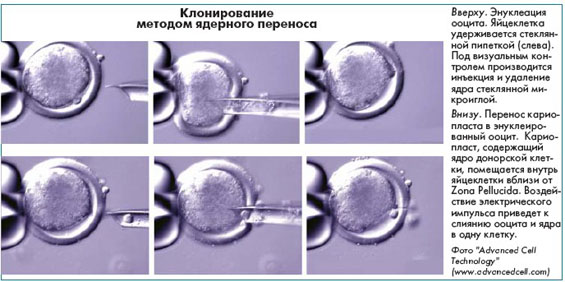
Метод ядерного переноса заключается в перемещении ядра из диплоидной, полностью укомплектованной парными хромосомами клетки, в неоплодотворенную яйцеклетку (ооцит) с предварительно удаленным материнским
ядром. В ооцит может быть перемещено изолированное ядро или кариопласт - донорское ядро вместе с окружающей цитоплазмой и плазматической мембраной. В последнем случае "реконструированный эмбрион" активируется, например, коротким электрическим импульсом.
Эмбрионы, как правило, культивируются в течение 5-6 дней. Развивающиеся нормально (обычно около 10%) имплантируются суррогатным матерям. Именно таким путем была получена Долли, и именно вокруг этого направления клонирования и развернулись бурные дискуссии.

Историческая справка
Любая дифференцированная клетка, имеющая ядро, обладает полным набором генов, необходимых для формирования целого организма. Однако в процессе дифференцировки часть генов "выключается" и функционально активными остаются только те, которые определяют свойства данной ткани. У животных в ходе эмбриогенеза клетки обособляются
довольно рано и только в процессе полового размножения, при котором происходит слияние мужской и женской гамет, образуется зигота (первая стадия развития зародыша), способная дать начало как целому организму, так и дифференцироваться в клетки любого вида ткани.
На протяжении довольно длительного времени ученые пытались решить вопрос, является ли сужение функций ядра дифференцированной клетки процессом необратимым. Еще в 1938 году немецкий ученый Hans Spemann предложил перенести ядро дифференцированной клетки в яйцеклетку, собственное ядро которой предварительно удалено. Однако в то время осуществить этот смелый эксперимент не удалось из-за отсутствия технических возможностей.
В пятидесятые годы прошлого века Robert Briggs из Institute of Cancer Research in Philadelphia (США) и Thomas J. King из New York University (США) осуществили перенос ядер клеток бластулы в энуклеированные яйцеклетки
леопардовой лягушки. Но ни в одном случае это не привело к нормальному развитию зародыша. В последующие годы ряд других исследователей предпринимали попытки клонирования амфибий, но неизбежно приходили к сходным результатам.
Казалось, что исследования зашли в тупик, однако причиной неудач была сама модель, выбранная для экспериментов. Развитие технологии микроманипуляций в то время еще не позволяло работать с эмбрионами млекопитающих, а яйцеклетка амфибии примерно в 1000 раз превышает размеры ооцита плацентарных животных.
Проблема клонирования амфибий остается нерешенной и по сей день, однако проведенные на них эксперименты позволили доказать, что ядра различных дифференцированных клеток одного организма генетически идентичны, а серийные пересадки ядер и культивирование клеток in vitro повышают потенцию ядер к обеспечению нормального развития реконструированных эмбрионов.
В семидесятых годах двадцатого века имелись все технические предпосылки для начала экспериментов по клонированию млекопитающих. Наиболее удобными объектами считались на то время мелкие лабораторные животные
- мыши и кролики. Ученым впервые удалось осуществить перенос ядра в яйцеклетку кролика с помощью микроинъекции, а также методом слияния бластомеров с овулированными ооцитами (слияние индуцировалось действием инактивированного вируса Сендай).
В 1986 году доктор Steen Willadsen из Institute of Animal Physiology in Cambridge (Англия) опубликовал результаты клонирования овец методом пересадки ядер бластомеров от 8- и 16-клеточных эмбрионов. В качестве реципиента ученый использовал энуклеированный ооцит, продемонстрировав, что яйцеклетка предоставляет пересаженному донорскому ядру больше времени для адаптации и репрограммирования в цитоплазме.
Доктор Neal First из University of Wisconsin (США) в 1987 году получил здоровых телят после имплантации в матку коровы эмбрионов с трансплантированными пронуклеусами зигот. К этому времени уже было установлено, что индуцирование переноса клеточного ядра в цитоплазму энуклеированного реципиента (зиготы или ооцита) с помощью электрического импульса в десять раз эффективнее, чем использование вируса Сендай.
Революционным в эмбриологии можно считать достижение ученых во главе с доктором Ian Wilmut из Roslin Institute (Шотландия), которым удалось получить в 1996 году первую клонированную овцу из соматической клетки взрослого животного. В качестве источника донорских ядер использовали клетки ткани молочной железы шестилетней овцы.
Трансплантация ядер осуществлялась после 3-6-го пассажа в энуклеированные ооциты. Всего было реконструировано 277 эмбрионов, из которых получили и перенесли в матку животных-реципиентов 29 морул и бластоцист. В результате развилась только одна нормальная беременность, завершившаяся рождением здорового ягненка.
В последующем появились сообщения о клонировании мышей (Wakayama, et al., 1998), коз (Baguisi, et al., 1999), обезьян вида макака резус (Chan, et al., 2000), свиней (Onishi, et al., 2000; Polejaeva, et al., 2000).
И еще одно знаменательное событие в истории клонирования. В 1999 году исследователи из Kyunghee University Hospital (Южная Корея) впервые сообщили об успешном клонировании человеческой клетки с помощью ядерного переноса, но, учитывая юридические и этические аспекты проблемы, ученые прервали эксперимент на стадии четырехклеточного эмбриона, не имплантировав его в матку суррогатной матери.
Проблемы
Несмотря на большое количество сообщений о получении новых клонов с помощью ядерного переноса, достижения в этой области продолжают оставаться невысокими. Официально только 1-3% "реконструированных эмбрионов" выживают. Большинство клонированного потомства погибает в последние недели беременности или сразу же после рождения, в основном из-за дыхательных или сердечно-сосудистых расстройств.
Количество спонтанных абортов после переноса реконструированных эмбрионов в 10 раз больше, чем при естественном оплодотворении. Анормальное развитие плаценты является одной из главных причин гибели плода на ранних сроках беременности. У абортированных плодов находят различную патологию: гипертрофированную плаценту,
гидроаллантоис, плацентомы, увеличенные в размере кровеносные сосуды пупочного канатика, отечность плодных оболочек. Для клонов, погибших в течение нескольких дней после рождения, характерно наличие патологии сердца, легких, почек, мозга. У новорожденных животных часто встречается так называемый "синдром крупного молодняка". Предполагается, что клонированные организмы склонны к ускоренному старению.
Изучение фундаментальных основ генной экспрессии и генетического контроля развития позволило объяснить причины негативных явлений, с которыми столкнулись ученые. Чтобы успешно реализовать генетическую информацию, ядро соматической клетки после трансплантации должно быстро репрограммироваться для экспрессии генов, включаемых на ранних этапах развития.
У клонированных животных из-за неполного репрограммирования ядра соматической клетки и нарушения экспрессии импринтированных генов возникает эпигенетическая нестабильность генома.
Несоответствующий данному гену уровень метилирования изменяет его активность и может приводить к полной инактивации. Последние исследования,
проведенные специалистами Whitehead Institute for Biomedical Research, еще раз подтвердили, что у клонированных из дифференцированной соматической клетки животных существует высокая вероятность нарушения экспрессии генов.
Известно, что для нормального развития эмбрионов мышей исключительно важным является ген Oct4, стимулирующий развитие плюрипотентных клеток, из которых формируются различные ткани организма. Всего же сотрудники института обнаружили более 60 генов, активность которых необходима для нормального развития эмбрионов. По крайней мере 10 из них несут функции, подобные Oct4.
Наблюдение за генетической активностью клонов, полученных из соматической клетки, показало, что только у 62% животных отмечалась правильная экспрессия всех десяти генов. Именно с нарушением активации генов ученые связывают большинство проблем выживания и развития клонов.
Преждевременное старение некоторых клонированных животных исследователи объясняют укорочением концевых участков хромосом - теломеров. Процесс репликации ДНК при делении клеток происходит таким образом, что теломеры в течение жизни человека или животного укорачиваются.
Существует фермент теломераза, который достраивает концевые участки хромосом, однако высокой теломеразной активностью обладают только тотипотентные клетки на ранних стадиях эмбрионального развития в период повышенного
количества митозов и герминальные, которые дают начало гаметам. Так как при трансплантации ядер донором служат соматические клетки, не экспрессирующие теломеразу, генетический возраст клонального животного определяется статусом теломеров на момент реконструкции эмбриона.
Улучшить результаты клонирования нелегко. В настоящее время есть только один способ достоверной оценки "качества" эмбриона - наблюдение под микроскопом. Большие усилия прилагаются для определения путей улучшения репрограммирования ядра: изучаются механизмы экспрессии генов, разрабатываются новые методы определения отклонений в развитии "реконструированных эмбрионов".
Перспективные направления. Клонирование животных
Технология ядерного переноса может быть использована для решения широкого спектра задач, не связанных с медициной. Клонирование элитных пород сельскохозяйственных и воспроизведение исчезающих
видов животных вполне осуществимо на сегодняшний день. Несмотря на высокую себестоимость метода (одна клонированная корова ценной породы стоит на аукционе в США более 40 000 долларов), биотехнологические компании продолжают работы в этом направлении.
В апреле 2003 года представители "Advanced Cell Technologies" сообщили об успешной попытке клонирования бантенгов (исчезающий вид диких быков) из клеток животного, умершего 23 года назад. Для ядерного переноса был использован генетический материал из банка тканей животных зоопарка Сан-Диего. Всего было реконструировано 45
эмбрионов, которых имплантировали тридцати обычным коровам. В последствии было сохранено 16 беременностей, из которых только две закончились родами. К сожалению, одного из двух телят, имевшего аномалии развития, характерные для клонированных животных, пришлось вскоре усыпить. У другого животного не было выявлено никаких отклонений от нормы.
Производство белков
Существующие на сегодняшний день методы получения человеческих протеинов имеют ряд существенных недостатков. В то же время большое количество белков можно получать из молока трансгенных животных, несущих человеческие гены, ответственные за выработку определенного протеина. Предполагается, что выход может составить до 40 г белка из одного литра молока при относительно невысокой стоимости.
Первое известие о рождении трансгенного животного в результате применения технологии клонирования датируется 1997 годом, когда Ian Wilmut с коллегами сообщили о рождении Полли - первой овцы, несущей в своих клетках человеческий ген.
Эксперименты по созданию трансгенных животных активно продолжаются. Так, исследователи компании "PPL Therapeutics" в 2001 году приступили к третьей фазе клинических испытаний альфа-1-антитрипсина, полученного от трансгенных животных и предназначенного для лечения фиброза мочевого пузыря и эмфиземы.
Ксенотрансплантация
Хронический дефицит человеческих органов для трансплантации вынуждает ученых искать другие альтернативные источники тканей. Только в США в базе данных United Network for Organ Sharing на сегодня зарегистрировано более 81 тыс. человек, нуждающихся в пересадке органов.
Ряд исследовательских центров работают над выведением генетически модифицированных поросят, органы которых могут быть использованы для трансплантации. С помощью ядерного переноса можно получить животных, у которых отсутствует ген a-galactosyltransferase, кодирующий фермент, ответственный за выработку на поверхности клеток свиньи углеводов, являющихся поверхностными антигенами и приводящими к реакции отторжения немедленного типа.
В августе 2002 года компания "PPL Therapeutics" объявила о клонировании пяти поросят обычного размера, у которых отсутствуют обе копии генов a-galactosyltransferase.
В январе 2003 года появилось сообщение о двухмесячной миниатюрной свинье Голди, клонированной специалистами компании "US-based Immerge BioTherapeutics". Особенностью этой породы свиней является то, что их органы сходны по размерам с человеческими. Сейчас планируются клинические исследования совместимости тканей трансгенных свиней и приматов.
Однако следует отметить, что получение линии подобных животных, возможно, позволит решить только проблему немедленного отторжения, оставляя нерешенным "замедленный иммунный ответ", обус-ловленный воздействием на трансплантат белых кровяных клеток реципиента. Несмотря на многолетние исследования, пересадка человеку органов свиньи все еще является отдаленным проектом.
Терапевтическое клонирование
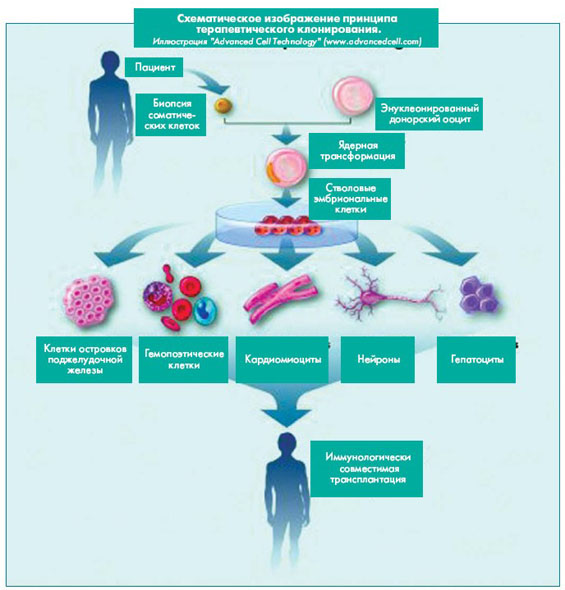
Терапевтическим клонированием называют пересадку ядер соматических клеток в энуклеированные яйцеклетки с целью получения культуры стволовых полипотентных эмбриональных клеток. Развитие эмбриона прерывается на ранних стадиях развития (чаще всего на стадии бластоцисты).
Полученная культура эмбриональных стволовых клеток подвергается воздействию веществ-индукторов, вызывающих направленную дифференциацию в определенный тип клеток, например в кардиомиоциты или в бета-клетки островков Лангерганса. Методы терапевтического клонирования позволяют избежать иммунного отторжения
трансплантатов, поскольку эмбриональные стволовые клетки несут генетическую информацию организма, от которого получены ядра, то есть самого пациента. Низкая эффективность ядерного переноса не так важна, так как для клеточной терапии используются эмбрионы на ранней стадии развития.
Основным препятствием на пути развития технологии явилось принятие в ряде стран законов, запрещающих клонирование человека, в том числе терапевтическое клонирование человеческих эмбрионов. Именно поэтому в настоящее время изучаются возможности использования в качестве цитопластов энуклеированных яйцеклеток животных, например крупного рогатого скота, которые поддерживают реализацию генетического материала ядра человеческой соматической клетки до стадии 5-дневного эмбриона.
Предполагается, что стволовые клетки, полученные методом терапевтического клонирования, можно будет использовать для лечения инсульта, инфаркта миокарда, переломов костей, цирроза печени. В настоящее время большинство исследований в этой области находится на стадии экспериментов.
Клонирование человека
Несмотря на внушительное количество проблем, сопутствующих клонированию, ряд специализирующихся в области биотехнологии ученых и компаний не оставляют попыток клонирования человека.
В конце 2002 года биотехнологическая фирма "Clonaid" сделала сенсационное заявление о рождении клонированного ребенка. Затем последовали новые сообщения о появлении человеческих клонов. Представители "Clonaid" заявляют, что все клонированные дети (их, якобы, пять) живы и чувствуют себя прекрасно. Однако до настоящего времени не было представлено реальных доказательств существования человеческих клонов. Компания ни разу не выполнила обещания представить детей для обследования и генетической экспертизы.
По мнению ведущих экспертов в области клонирования, эти сообщения являются ложными и направлены на увеличение доходов компании и повышение популярности секты Раэля, которая и создала "Clonaid".
Впрочем, дыма без огня не бывает, первый клонированный ребенок рано или поздно в нарушение всех запрещающих законов и этических норм появится на свет. По мнению известного российского генетика, вице-президента РАМН Николая Бочкова, клонирование человека на нынешнем уровне развития науки в принципе возможно. Процесс ввода ядра соматической клетки в цитоплазму яйцеклетки отработан на животных. Развитие будущей зиготы будет
требовать определенного состава среды, но это техническая сторона, которую экспериментально возможно отрегулировать. Дальнейшая процедура деления клетки с образованием зародышевых пузырьков будет примерно такой же, как при экстракорпоральном оплодотворении. Главная проблема репродуктивного клонирования - не техника его осуществления, а неизвестность последствий, к которым оно приведет.
Литература
1. Гоголевский П.А., Здановский В.М. Клонирование (обзор литературы) // Журнал "Проблемы репродукции", №3 (1998) http://www.rusmedserv.com/article/articleprint/85/-1/29/
2. Смирнов Ф. Такое разное клонирование...//Медицинская газета, № 14 (2003 г.) //http://medgazeta.rusmedserv.com
3. Шкуматов А.А. Клонирование: прошлое, настоящее... будущее? // Журнал "Проблемы репродукции", №6 (2001) http://64.191.10.157:1337/article/articleview/467/1/56/
4. Alex Bortvin, Rudolf Jaenisch, David Page. Inactive Genes May Contribute to Failure of Animals Cloned from Adult Cells, Study Finds //Whitehead Institute //http://www.wi.mit.edu
5. Bert Thompson, Ph.D. and Brad Harrub, Ph.D. Human Cloning and Stem-Cell research - Scence's "Slippery Slope", Reason & Revelation, August 2001, 21[8]:57-63 // http://www.apologeticspress.org/rr/rr2001/r&r0108a.htm
6. Mammalian Cloning: Advances and Limitations, Nature Reviews Genetics 1; 199-207 (2000);// www.nature.com
7. Advanced Cell Technology //www.advancedcell.com
8. PPL Therapeutics //www.ppl-therapeutics.com
9. Roslin Institute //www.roslin.ac.uk
10. www.NewScientist.com; www.medscape.com; http://news.bbc.co.uk; http://europe.cnn.com; www.unos.org; www.reproductivecloning.net
Medicus Amicus 2003, #5
|
|















 Новости
Новости 