Гемолитико-уремический синдром у детей
Борисова Т.П., доктор медицинских наук,
профессор кафедры педиатрии Донецкого государственного медицинского университета им. М.Горького,
заместитель главного редактора «Medicus Amicus»
Термин гемолитико-уремический синдром (ГУС) впервые использован Gasser в 1955 г., поэтому в литературе также встречается термин болезнь Гассера. ГУС определяется триадой симптомов: микроангиопатическая гемолитическая анемия, почечная недостаточность и тромбоцитопения.
В настоящее время ГУС является одной из частых причин острой почечной недостаточности (ОПН) у детей раннего возраста, своевременность постановки диагноза и лечения определяет исход заболевания.
Этиология. ГУС встречается у детей и взрослых. В грудном и раннем возрасте он имеет клинико-патогенетические особенности, что позволяет говорить о его нозологической самостоятельности именно как о болезни. У взрослых он наблюдается редко и рассматривается как синдром. Установлена связь ГУС с применением оральных контрацептивов, кокаина, некоторых лекарств (циклоспорин А, митомицин С, хинин), с беременностью, опухолями, трансплантацией костного мозга, системной красной волчанкой (антифосфолипидный синдром), СПИДом.
В детском возрасте самыми частыми причинами ГУС являются диарея (90 %) и инфекция верхних дыхательных путей (10 %). Этиологический фактор должен обладать способностью повреждать эндотелиальные клетки. Такими свойствами наделены шига-подобный токсин или веротоксин, продуцируемый Escherichia coli O157:H7, Shigella dysenteriae type І, Aeromonas hydrophilia, а также нейраминидаза Streptococcus pneumoniae. Кроме этого, развитие ГУС вызывают не образующие веротоксин бактерии – Salmonella, Campylobacter, Yersinia, Clostridium difficile, вирусы ветряной оспы, ECHO, Коксаки А и B. Некоторые исследователи предполагают, что ГУС также связан с иммунными комплексами. Описаны семейные случаи ГУС, как доминантный, так и рецессивный тип аутосомного наследования. У этих больных выявлено снижение продукции эндотелиальными клетками простациклина (эндогенного ингибитора агрегации тромбоцитов).
У детей в 70-85 % случаев причиной ГУС является E. coli O157:H7-инфекция, приводящая к развитию диареи. Патогенная для человека E.coli О157:Н7 находится в кишечнике здоровых кошек и крупного рогатого скота, передача которой происходит при контакте с животными, употреблении пищи (говяжьего фарша и других мясных изделий), не прошедшей достаточной термической обработки. Бактерии могут быть в непастеризованных молочных продуктах и фруктовых соках, нехлорированной воде. Следует отметить, что пища, загрязненная E.coli, не имеет неприятного запаха и вкуса. Инфицирование ребенка может произойти при посещении зоопарка и контакте с больным диареей.
Приблизительно 10-15% детей, инфицированных E. coli O157:H7, заболевают ГУС, риск развития которого увеличивается в случае лечения диареи антиперистальтическими препаратами, амоксициллином или его сочетанием с гентамицином, триметоприм-сульфаметаксазолом.
Течение и прогноз ГУС связаны с этиологическим фактором. Выделяют 2 формы ГУС: типичный ГУС – диарея плюс ГУС (Д+ГУС), атипичный ГУС – диарея минус ГУС (Д?ГУС). Последняя форма отмечается в 10 % случаев.
Эпидемиология. ГУС встречается во всем мире. Ежегодная частота у детей до 5-летнего возраста составляет 2-3, до 18-летнего – 0,97 случаев на 100 000 детского населения. Заболеваемость ГУС имеет тенденцию к сезонному колебанию с максимумом в теплое время года (июнь–сентябрь). ГУС характерен для грудного и раннего возраста (от 6 мес. до 4 лет). Возрастная зависимость не прослеживается при форме Д?ГУС.
Патогенез. E. coli вызывает повреждение кишечника и поступление в циркуляцию веротоксина. Последний действует на клетки, имеющие специфические ветороксин-рецепторы, которые обнаружены в эндотелии почек, кишечника, ЦНС, нейтрофилах, моноцитах. Наибольшее скопление таких рецепторов отмечено в эндотелии гломерул и мезангии почек. В результате эндоцитоза веротоксин проникает в клетку и приводит к блокаде синтеза белка (цитотоксическое действие). Кроме этого, липополисахариды E. coli стимулируют синтез цитокинов (интерлейкинов IL-1, TNF), активизируют нейтрофилы с образованием протеаз, что усиливает повреждение эндотелия.
В результате повреждения эндотелиальных клеток наступает каскад событий, которые завершаются образованием тромбоцит-фибрин-гиалиновых микротромбов, закрывающих мелкие артерии и капилляры. При ГУС гиалиновые тромбы в основном находятся в афферентной артериоле и гломерулярных капиллярах. В результате сужения или облитерации их просвета снижается скорость клубочковой фильтрации, уменьшается перфузия почечных канальцев, развивается их вторичная дисфункция или некроз. У части больных течение ГУС характеризуется вовлечением в процесс многих органов и систем. Это объясняется тем, что тромботическая микроангиопатия поражает не только сосуды почек, но и головного мозга, кишечника, печени, поджелудочной железы, легких, сердца.
Тромбоцитопения и гемолитическая анемия обусловлены микроангиопатией: повышенное потребление тромбоцитов из-за их агрегации и разрушения, механическое повреждение эритроцитов во время продвижения по измененной капиллярной сети.
Морфология. Макроскопически почки отечные, бледные с множеством кровоизлияний на поверхности. Васкулит обычно отсутствует. Гистологически в клубочках обнаруживаются набухшие эндотелиальные клетки. Они отделены от базальной мембраны субэндотелиальной полоской, содержащей вещество, в состав которого входят фибрин, тромбоциты, фрагменты эритроцитов. Мезангий расширен. В капиллярах клубочков и мелких артериях определяются микротромбы. Это приводит к острому корковому некрозу, вовлекающему гломерулы и канальцы. Патологические изменения в головном мозге детей, умерших от ГУС, неспецифичны (отек, некроз клеток); микротромбы обнаружены лишь в нескольких случаях.
В отдаленном катамнезе у пациентов со стойкой протеинурией и артериальной гипертензией при нефробиопсии отмечается гломерулосклероз.
Клиника. Продромальный период длится 2-14 (в среднем 6) дней и характеризуется эпизодом диареи с примесью крови. Начало ГУС сопровождается ухудшением общего состояния ребенка, нарастанием вялости и бледности кожных покровов, у части больных приобретающих иктеричный оттенок. Лихорадка присутствует у 5-20% пациентов. Отмечается снижение диуреза, появление пастозности век, голеней и азотемии. У 50-70% детей с Д+ГУС развивается олигоанурическая ОПН. Наблюдается стойкая артериальная гипертензия.
При тяжелом течении ГУС наблюдаются экстраренальные поражения. Возможно вовлечение в процесс ЦНС (судороги, кома, корковая слепота), сердца (ишемия с развитием недостаточности, аритмии), легких (кровоизлияния, отек), любого отдела ЖКТ (эзофагит, энтероколит, некроз, перфорация, инвагинация кишечника, гепатит, панкреатит). У единичных больных встречается кровоизлияние в сетчатку глаза или стекловидное тело.
Анемия характеризуется внезапным началом, быстрым снижением гемоглобина до 60-80 г/л, иногда до критических цифр (30-40 г/л), с ретикулоцитозом, анизоцитозом. Кроме этого, отмечается лейкоцитоз.
Тромбоцитопения умеренная, иногда бывает кратковременной или рецидивирующей, может привести к появлению петехий (у 15-18% пациентов), но обычно протекает без кровотечений.
 Диагностике ГУС помогает микроскопическая картина крови, позволяющая выявить фрагментированные эритроциты (рис. 1). Степень анемии и тромбоцитопении не коррелирует с тяжестью почечной дисфункции. В периферической крови могут быть гигантские тромбоциты. Диагностике ГУС помогает микроскопическая картина крови, позволяющая выявить фрагментированные эритроциты (рис. 1). Степень анемии и тромбоцитопении не коррелирует с тяжестью почечной дисфункции. В периферической крови могут быть гигантские тромбоциты.
Плазма содержит свободный гемоглобин, который можно выявить макроскопически. Прямая и непрямая реакция Кумбса имеет отрицательный результат. В костном мозге наблюдаются эритроидная гиперплазия, увеличение количества мегакариоцитов.
Отмечаются умеренная и транзиторная непрямая гипербилирубинемия, значительное повышение мочевины и креатинина крови. Трансаминазы крови могут быть несколько повышены. Уровень комплемента крови (C3 и C4) снижен. Гаптоглобин значительно снижен.
Электролитные нарушения (гипонатриемия, гиперкалиемия), ацидоз выявляются в олигоанурической стадии ОПН.
Коагулопатия по лабораторным данным отсутствует. Это свидетельствует о том, что при развернутой клинической картине ГУС активное отложение фибрина уже закончилось. Протромбиновое время, частичное активированное тромбопластиновое время и фибриноген крови – в пределах нормы. Может отмечаться снижение уровня антитромбина-ІІІ, умеренный фибринолиз с небольшим повышением продуктов деградации фибрина.
В анализе мочи обнаруживается протеинурия от незначительной до выраженной, эритроцитурия вплоть до макрогематурии, гемоглобинурия, гемосидеринурия.
При ультразвуковом исследовании почки увеличены, повышенная эхогенность паренхимы. Существенные изменения наблюдаются при ультразвуковой доплерографии почечных сосудов.
В обследовании детей необходимо предусмотреть бактериологическое исследование кала, с обязательным посевом на ?E. coli? O157:H7.
Течение. Продолжительность ГУС различна и зависит от его тяжести. При среднетяжелом течении диурез не меняется, снижение функции почек умеренное. Тяжелое течение ГУС приводит к анурии, требующей диализа, и развитию экстраренальных поражений. Наличие лихорадки и лейкоцитоза – критерий риска развития тяжелого ГУС.
Обычная длительность ГУС 1-2 недели, затем наступает стабилизация и постепенное восстановление. Вначале наблюдается повышение уровня тромбоцитов, затем улучшение выделения мочи и в последнюю очередь разрешение анемии. Гемоглобин чаще нормализуется спустя 1 месяц после улучшения состояния.
Терапия. В настоящее время осуществляется поддерживающее лечение, направленное на сохранение гематокрита в приемлемых пределах, нормализацию содержания электролитов в сыворотке и поддержание водного баланса, а также на борьбу с артериальной гипертензией и судорогами. Показана высококалорийная диета с ограничением соли. При отечном синдроме применяют мочегонные средства (фуросемид), при тахикардии – бета-адреноблокаторы. При тяжелой гипертензии предпочтительна непрерывная инфузия нитропруссида натрия с постоянным АД-мониторингом. При сохранении гипертензии в дальнейшем показан оральный прием гипотензивных средств.
Осуществляется ежедневный контроль за гематокритом. Если гематокрит менее 20 %, гемоглобин менее 60 г/л, переливают эритроцитную массу. Переливание тромбоцитарной массы может ухудшить состояние пациента, вызывая дальнейшее повреждение почек, поэтому к нему прибегают лишь в случае значительных кровотечений или хирургического вмешательства.
Около 50% пациентов с типичным ГУС нуждаются в диализе (перитонеальный или гемодиализ), причем в раннем его начале. Показания к назначению: олигурия, резистентная к мочегонным средствам, выраженные гипергидратация, гиперкалиемия, гипонатриемия, ацидоз.
Некоторые авторы предлагают проведение плазмафереза с трансфузией свежезамороженной плазмы при Д–ГУС, а также в случае длительной анурии (более 2 недель) или тяжелых осложнений со стороны ЦНС при Д+ ГУС.
Лечение антибиотиками Д+ГУС остается спорным. Их применение может увеличить риск развития ГУС у детей с? диареей, поскольку в этой ситуации увеличивается продукция веротоксина.
Согласно мнению редакционного совета JAMA, на сегодняшний день нет весомых доказательств пользы применения антибактериальных препаратов для профилактики или лечения ГУС. Многие практикующие врачи, вероятно, не согласятся с этим заключением и будут придерживаться тактики терапии ГУС, основанной на их клиническом опыте.
Число проспективных контролируемых исследований эффективности антикоагулянтной терапии невелико. У большинства детей выздоровление наступает без ее применения. Данный вид терапии сопряжен со значительным риском геморрагических осложнений. Некоторые авторы указывают, что антикоагулянтная терапия не дает немедленного антитромботического эффекта, но способна в тяжелых случаях оказывать продолжительное благоприятное влияние на гипертензию и протеинурию.
Кортикостероиды, антитромбоцитарные (дипиридамол) и антиоксидантные средства также имеют сомнительную эффективность.
Использование внутривенного иммуноглобулина (2 г/кг массы внутривенно 2-5 дней) в одном исследовании при тяжелом ГУС с поражением ЦНС показало более быстрое выздоровление пациентов.
В настоящее время ведется поиск средств, способных связать веротоксин в кишечнике и предотвратить ГУС. Один из них– SYSNSORB Pk прошел испытания, но еще не доступен для клинического применения.
Исходы и прогноз. Исходом острой стадии ГУС при благоприятном течении является полиурическая стадия ОПН, которая продолжается 1-1,5 месяца. Летальность при адекватной помощи составляет 5-15%, в слаборазвитых странах – до 70 %, при наследственном ГУС – 70-90 %. при рецидивах ГУС – 30 %. Причина летальных исходов – поражение ЦНС, сердечная или полиорганная недостаточность.
Долгосрочные исследования показали, что 70-85% пациентов восстанавливают почечную функцию. Стойкость гипертонии или протеинурии спустя 1 год после ГУС указывает на риск хронической почечной недостаточности (ХПН). Через 5-7 лет ХПН развивается у 5%, через 10-15 лет – еще у 10-25% больных.
Неблагоприятными прогностическими признаками являются: раннее появление анурии и ее длительность более 2 недель, прогрессирующее поражение ЦНС, микротромбы более чем в 60 % гломерул, лейкоцитоз более 20x109/л, атипичная форма ГУС, возраст до 6 месяцев и старше 4 лет.
Дети, перенесшие ГУС, нуждаются в контроле артериального давления, креатинина сыворотки, анализа мочи (уровня протеинурии). Пациентам с постоянной гипертонией показано назначение гипотензивных препаратов (ингибиторов АПФ).
Лучшими способами профилактики ГУС являются качественная кулинарная обработка пищевых продуктов, особенно мясных, личные меры гигиены (мытье рук, исключение купания в грязных водоемах), уменьшение фекального загрязнения мяса во время или после убоя животных.
Литература
1 Зверев Д.В., Теблоева Л.Т. Гемолитико-уремический синдром как ведущая причина острой почечной недостаточности у детей раннего возраста. – Нефрология и диализ. – 2000. – Т.2.– №4.– С.317-321
2 Biega T. Hemolytic-Uremic Syndrome. – www/emedicine.com –
Last Updated: June 27, 2006
3 Garg A.X., Suri R.S., Barrowman N. et al/ Long-term Renal Prognosis of Diarrhea-Associated Hemolytic Uremic Syndrome. A Systematic Review, Meta-analysis and Meta-regression. – JAMA. – 2003. – V.290. – Р. 1360-1370.
4 Kaplan B.S., Cleary T.G., Obrig T.G. Recent advances in understanding of the hemolytic uremic syndrome. – Pediatr. Nephrol. – 1990. – № 4. – Р.276-283.
5 Safdar N., Said A., Gangnon R.E., Maki D.G. Risk of Hemolytic Uremic Syndrome After Antibiotic Treatment of Escherichia coli O157:H7 Enteritis: A Meta-analysis. – JAMA – 2002. – V.288. – P. 996-1013.
6 Shapiro W. Hemolytic Uremic Syndrome. – www/emedicine.com
Last Updated: July 13, 2006
Medicus Amicus, №6 2006
|















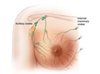 Пожилой возраст является фактором риска при раке молочной железы (РМЖ). Большая часть смертей от РМЖ происходит именно у пожилых. Не всегда у них удается провести лечение сог..
Пожилой возраст является фактором риска при раке молочной железы (РМЖ). Большая часть смертей от РМЖ происходит именно у пожилых. Не всегда у них удается провести лечение сог.. включала всех живорожденных детей, а также случаи мертворождения и прерывания беременности вследствие врожденных пороков в 7 канадских провинциях за период 1993 по 2002 гг. Основн..
включала всех живорожденных детей, а также случаи мертворождения и прерывания беременности вследствие врожденных пороков в 7 канадских провинциях за период 1993 по 2002 гг. Основн..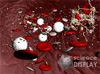 Роль антитромботической терапии при хронической сердечной недостаточности (ХСН) у пациентов с синусовым ритмом обсуждается много лет. В частности, оживленные дискуссии вызывает воп..
Роль антитромботической терапии при хронической сердечной недостаточности (ХСН) у пациентов с синусовым ритмом обсуждается много лет. В частности, оживленные дискуссии вызывает воп.. Жаропонижающие лекарственные средства - препараты, наиболее часто используемые для лечения детей как педиатрами, так и родителями. Этому способствуют бытующие представления об опас..
Жаропонижающие лекарственные средства - препараты, наиболее часто используемые для лечения детей как педиатрами, так и родителями. Этому способствуют бытующие представления об опас.. Неонатальный сепсис (НС) остается ведущей причиной смерти у недоношенных новорождённых. Стратегии для уменьшения частоты НС по-прежнему не достаточно эффективны, и связанная с НС с..
Неонатальный сепсис (НС) остается ведущей причиной смерти у недоношенных новорождённых. Стратегии для уменьшения частоты НС по-прежнему не достаточно эффективны, и связанная с НС с.. Диагностике ГУС помогает микроскопическая картина крови, позволяющая выявить фрагментированные эритроциты (рис. 1). Степень анемии и тромбоцитопении не коррелирует с тяжестью почечной дисфункции. В периферической крови могут быть гигантские тромбоциты.
Диагностике ГУС помогает микроскопическая картина крови, позволяющая выявить фрагментированные эритроциты (рис. 1). Степень анемии и тромбоцитопении не коррелирует с тяжестью почечной дисфункции. В периферической крови могут быть гигантские тромбоциты.
 Новости
Новости 