Может ли улыбка улучшить настроение?
Улыбка на лице не всегда влияет на наши эмоции...
| 11 имплантируемых устройств, которые скоро будут у вас в теле.
Все вокруг обсуждают, как изменится мир с повсеместным использованием носимых электронных устройств - коммуникационных, медицинских, геопозиционных и т.п. Но мы полагаем, что эти т..
| Адъювантная химиотерапия при ранних стадиях рака молочной железы у пожилых больных: стандартные схемы эффективнее капецитабина.
 Пожилой возраст является фактором риска при раке молочной железы (РМЖ). Большая часть смертей от РМЖ происходит именно у пожилых. Не всегда у них удается провести лечение сог.. Пожилой возраст является фактором риска при раке молочной железы (РМЖ). Большая часть смертей от РМЖ происходит именно у пожилых. Не всегда у них удается провести лечение сог..
| Нормальное содержание фолиевой кислоты в организме женщины детородного возраста снижает риск развития пороков нервной трубки у детей.
 включала всех живорожденных детей, а также случаи мертворождения и прерывания беременности вследствие врожденных пороков в 7 канадских провинциях за период 1993 по 2002 гг. Основн.. включала всех живорожденных детей, а также случаи мертворождения и прерывания беременности вследствие врожденных пороков в 7 канадских провинциях за период 1993 по 2002 гг. Основн..
| Сравнительная эффективность антитромботических режимов при хронической сердечной недостаточности. Данные исследования WATCH
 Роль антитромботической терапии при хронической сердечной недостаточности (ХСН) у пациентов с синусовым ритмом обсуждается много лет. В частности, оживленные дискуссии вызывает воп.. Роль антитромботической терапии при хронической сердечной недостаточности (ХСН) у пациентов с синусовым ритмом обсуждается много лет. В частности, оживленные дискуссии вызывает воп..
| О безопасном применении жаропонижающих средств у детей
 Жаропонижающие лекарственные средства - препараты, наиболее часто используемые для лечения детей как педиатрами, так и родителями. Этому способствуют бытующие представления об опас.. Жаропонижающие лекарственные средства - препараты, наиболее часто используемые для лечения детей как педиатрами, так и родителями. Этому способствуют бытующие представления об опас..
| Гранулоцитарно-макрофагальный колониестимулирующий фактор не снижает частоту сепсиса и не улучшает выживание глубоко недоношенных младенцев
 Неонатальный сепсис (НС) остается ведущей причиной смерти у недоношенных новорождённых. Стратегии для уменьшения частоты НС по-прежнему не достаточно эффективны, и связанная с НС с.. Неонатальный сепсис (НС) остается ведущей причиной смерти у недоношенных новорождённых. Стратегии для уменьшения частоты НС по-прежнему не достаточно эффективны, и связанная с НС с..
|
| `Шок: патофизиология и принципы лечения
виды шока патофизиология шока принципы лечения шока
Шок: патофизиология и принципы лечения
Глотов М.А., ассистент кафедры анестезиологии и реанимации Крымского государственного медицинского университета им. С.И. Георгиевского
В той или иной мере с шоковыми состояниями приходится сталкиваться врачу любой специальности. При этом от своевременности и правильности его действий зачастую зависит
жизнь пациента. Эволюция представлений о шоке продолжается уже второе столетие. Изначально термин "шок" употреблялся для описания крайне тяжелой формы течения механической травмы, впоследствии им стали обозначать общую реакцию организма на повреждение, придавая
ведущее значение в патогенезе данного состояния нервной системе. В дальнейшем развитие фундаментальных медицинских дисциплин позволило расширить круг состояний, попадавших под определение "шок".
Точкой их соприкосновения оказались характерные нарушения в системе макро- и микроциркуляции. Они наблюдаются на определенном этапе течения как хирургических, так и терапевтических заболеваний - на том этапе, когда болезнь превращается в критическое состояние и патогенез становится танатогенезом. В настоящее
время "шок" - собирательное понятие, при этом, несмотря на общие механизмы формирования гемодинамических нарушений, клиническая картина и терапевтические мероприятия при разных формах шока существенно отличаются.
Для того чтобы понять, почему же столь разные по патогенезу и клинике состояния объединяются в одну категорию, необходимо сказать несколько слов о системе циркуляции крови в целом.
Важнейшей задачей сердечно-сосудистой системы (ССС) является обеспечение соответствия между потребностью тканей в кислороде и его доставкой. Потребность
в кислороде определяется целым рядом факторов (например, состоянием основного обмена, физической активностью и др.) и является весьма вариабельной величиной. В соответствии с потребностями организма меняется и величина кислородного транспорта. Транспорт кислорода - это многоступенчатый процесс, который зависит от работы не только ССС.
Для определения состояния кислородного транспорта используют такой показатель, как индекс кислородного потока, или системный транспорт кислорода - СТО2 (в англоязычной литературе аналогичный показатель обозначается DO2).
СТО2, мл/мин*м2 = 1,39*Нвo(SaO2/100)*СИ
где SaO2 - сатурация артериальной крови, или процент насыщения гемоглобина кислородом;
1,39 - константа Гюффнера, показывающая, что 1г гемоглобина может связать 1,39 мл кислорода;
Нв - содержание гемоглобина в сыворотке крови (г/л);
СИ - сердечный индекс - отношение количества крови, проходящей через сердце за минуту, или сердечного выброса (СВ), к площади поверхности тела.
Данная формула удачно демонстрирует вклад основных систем в общий процесс обеспечения организма кислородом, поскольку несет в себе сведения о возможностях дыхательной системы (SaO2), ССС (СИ) и глобулярного объема крови (Нв). Увеличение кислородного потока к тканям в основном осуществляется за счет сердечно-сосудистой системы.
Тахикардия - универсальный механизм увеличения СВ, быстро и значительно повышающий транспорт кислорода на периферию при возросших потребностях в нем.
В здоровом организме потребность органов и тканей в кислороде целиком обеспечивается за счет слаженной работы легких и ССС. Однако при целом ряде ситуаций (массивное кровотечение,
обширный инфаркт миокарда, анафилаксия и др.) возникает острое несоответствие между потребностью в кислороде и его доставкой на периферию. Это может быть обусловлено двумя группами причин:
1. Резко снижаются функциональные резервы ССС по обеспечению доставки кислорода к тканям.
2. Функциональные возможности ССС относительно сохранены, однако потребность организма в кислороде значительно повышена либо утилизация его тканями нарушена.
В обоих случаях дисбаланс в системе "доставка-потребление кислорода" ведет к прогрессирующей ишемии тканей. Наступает острая декомпенсированная циркуляторная недостаточность, или шок.
Термин "ишемия" обозначает абсолютную или относительную недостаточность объемного кровотока в тканях, что всегда сопровождается гипоксией различной выраженности.
Она приводит к смене аэробного окисления глюкозы на анаэробное, следствием чего является накопление в тканях значительного количества лактата и некоторых других кислых продуктов обмена. В результате повышается проницаемость капилляров и значительная часть циркулирующей плазмы выходит за пределы сосудистого русла, обеспечивая уменьшение объема циркулирующей крови (ОЦК),
или гиповолемию. Патофизиологические следствия гиповолемии разнообразны, но в первую очередь- это снижение венозного возврата к сердцу.
В соответствии с законом Франка - Старлинга гиповолемия способствует снижению силы сокращения миокарда с падением ударного объема и, соответственно, минутного объема кровообращения (МОК). Формируется один из т.н. порочных кругов, когда гиповолемия и ишемия потенцируют развитие друг друга.
Если этот круг не прервать извне и не оказать больному должной помощи, он погибнет.
Еще одним важнейшим следствием снижения МОК является изменение реологических свойств крови. Кровь представляет собой суспензию, вязкостные свойства которой зависят от скорости кровотока.
При падении МОК периферический кровоток замедляется, что в значительной степени повышает вязкость крови, нарушает её стабильность и вызывает феномен агрегации эритроцитов.
Агрегаты оказывают весьма неблагоприятное влияние на микроциркуляцию, поскольку содержат на своей поверхности адгезивные вещества, которые запускают процесс микротромбообразования. По этой причине при любом критическом состоянии всегда существует опасность развития ДВС - синдрома.
Кроме того, агрегаты "перекрывают" капилляры, тем самым вызывая ишемию кровоснабжаемых ими участков ткани. При длительных сроках существования тканевой ишемии возможно развитие секвестрации крови (оседание в капиллярах значительного количества клеток
крови и плазменных белков), что в еще большей степени усугубляет гиповолемию. Секвестрированная кровь не просто выключена из кровотока: она непригодна для организма, поскольку входящие в состав агрегатов клетки прочно соединены между собой белками и молекулярными связями.
Такая кровь может восстановить свои свойства, только пройдя через систему капилляров легких, которые наряду с обеспечением дыхания выполняют еще и ряд недыхательных функций
(очистка крови от механических примесей, участие в метаболизме многих биологически активных пептидов, регуляция системы свертывания крови и др.). Однако возможности легких не безграничны. При любом критическом состоянии в них устремляется
поток микроэмболов, агрегатов, клеточных фрагментов, биологически активных веществ, поэтому дыхательная недостаточность в том или ином виде так часто встречается в практике врача интенсивной терапии [2].
При некоторых формах шока (например при геморрагическом) возможно возникновение такого явления, как централизация кровообращения. Изначально централизация кровообращения
является защитной реакцией, направленной на преимущественное обеспечение органов и систем, ответственных за адаптацию (ССС, ЦНС). Главная роль в реализации этого эффекта принадлежит гуморальным факторам: катехоламинам, вазопрессину, ангиотензину II.
Эти вещества, вызывая сужение артериол и венул, на какое-то время повышают системное артериальное давление и увеличивают венозный возврат.
Однако артериолоспазм приводит к еще большему снижению объемного кровотока через капилляры заинтерессованных органов. В результате кровь, минуя капилляры, устремляется в артерио-венозные анастомозы. В даной ситуации может наблюдаться даже кратковременное повышение СВ, но это не может предотвратить нарастающую
ишемию тканей. В первую очередь при централизации кровообращения страдают печень, кишечник, почки и надпочечники, поэтому, если симптоматика шока сохраняется достаточно долго, с большой вероятностью можно ожидать поражения этих органов, чаще всего в виде возникновения острых эрозий и язв желудочно-кишечного тракта и/или острой почечной недостаточности.
Таким образом, шок - это собирательное название различных видов острой циркуляторной недостаточности, в основе которых всегда лежит синдром малого сердечного выброса с тотальной тканевой ишемией (К.М. Лебединский, 1999). Термин "циркуляторная" означает, что именно гемодинамические нарушения являются ведущими
в нарушении кислородного обеспечения организма. По этой причине к шокам не относят те случаи гипоксии, когда транспорт кислорода лимитирован дыхательной системой (массивная пневмония, синдром острого легочного повреждения) или системой гемоглобина (отравления угарным газом или метгемоглобинообразователями).
В данных ситуациях также может наблюдаться сердечная или сосудистая недостаточность, однако эти нарушения по отношению к развитию критического состояния являются вторичными. В остальном же механизмы формирования гиповолемии, нарушения реологических свойств крови и развития полиорганной недостаточности универсальны для всех критических состояний [2]!
До сих пор речь шла только об общих моментах патогенеза всех шоков. Между тем они не похожи один на другой в своем начальном развитии и для успешного лечения требуют применения
дифференцированной терапии. В зависимости от ведущего пускового механизма (уровня "поломки" ССС) можно выделить следующие группы шоков (табл.1):
Не все варианты шока однозначно можно отнести только к той или иной группе. В патогенезе критического состояния зачастую играет роль несколько факторов, один из которых обычно является ведущим.
Например, при анафилактическом шоке в результате повышенной проницаемости капилляров к относительной гиповолемии очень быстро присоединяется абсолютная. При септическом шоке, который отнесен в группу вазогенных,
на первый план очень часто выступают явления сердечной декомпенсации вследствие поражения миокарда бактериальным эндотоксином. Кроме того, уже на начальных стадиях развития септического шока, еще до развития ярких гемодинамических нарушений, под влиянием того же эндотоксина происходит нарушение утилизации кислорода органами и тканями.
Кислорода в притекающей крови достаточно, однако большая его часть проходит "мимо клеток". В результате развивается ситуация, когда ни при каком увеличении СВ не удается обеспечить нормальной оксигенации тканей: кислород просто не усваивается в должном количестве.
Диагностика шока основывается, в первую очередь, на клинических проявлениях заболевания. Для сравнения приведены диагностические критерии кардиогенного и септического шока (табл.2). Следует помнить, что уровень АД при шоке может и не отражать адекватности тканевой перфузии! Широко доступным в
клинической практике показателем состояния периферического кровотока является величина минутного диуреза. Снижение объемного органного кровотока при шоке начинается, как правило, с почек и органов спланхнической зоны. Поэтому первые признаки гипоперфузии проявляются именно там.
Нормальный диурез составляет в среднем 0,75-1 мл/кг в час; снижение почечного фильтрационного давления сопровождается явлениями олигурии. Величина минутного диуреза - довольно чуткий показатель состояния микроциркуляции, однако всегда необходима комплексная оценка всех клинических проявлений заболевания:
каждый шок сопровождается олигурией, но не всегда олигурия является признаком шока.
Если диагностика шока базируется прежде всего на клинических его проявлениях, то современные подходы терапии требуют применения дополнительных методов обследования пациента.
Для успешного лечения шоковых состояний необходимо определить состояние оксигенации тканей. В настоящий момент используется двухэтапный подход к ведению таких больных.
На первом этапе необходимо исследовать основные параметры гемодинамики с целью определения и коррекции ведущих нарушений. Как правило, из всего многообразия показателей работы ССС для этой цели достаточно определить три: СВ, общее периферическое сосудистое сопротивление (ОПСС) и давление заклинивания
легочных капилляров (ДЗЛК). СВ отражает производительность миокарда, ОПСС - тонус резистивных сосудов, ДЗЛК - преднагрузку на левые отделы сердца. В комплексе эти три параметра образуют т.н. малый гемодинамический профиль.
Например, для кардиогенного шока малый гемодинамический профиль будет выглядеть так: низкий СВ/высокое ДЗЛК/высокое ОПСС, для гиповолемического шока - низкий СВ/низкое ДЗЛК/высокое ОПСС и т.д.
В соответствии с получаемой информацией определяется дальнейшая тактика ведения пациента с использованием медикаментозных и немедикаментозных методов лечения.
Для определения параметров центральной гемодинамики было предложено много методов. В настоящее время в интенсивной терапии широко используются два из них. Наибольшее распространение в мире
получил метод термодилюции. Основные преимущества метода - высокая точность и возможность проведения мониторинга - непрерывного динамического наблюдения за больным.
К недостаткам метода относятся инвазивность (необходима катетеризация легочной артерии) и высокая стоимость аппаратуры и расходных материалов. Этих недостатков лишен реографический метод.
По точности он уступает термодилюционному, однако выгодно отличается от него неинвазивностью и относительно невысокой стоимостью. Кроме того, реография позволяет прослеживать изменения гемодинамики, что позволяет использовать ее для мониторинга.
Целью второго этапа является оценка первоначального эффекта терапии в отношении оксигенации тканей и достижения соответствия между потреблением кислорода тканями и уровнем метаболизма в них. С этой целью используются такие показатели, как доставка кислорода (DO2), потребление кислорода тканями (VO2)
и содержание лактата в сыворотке крови. Наиболее значимым показателем является VO2. Его низкие показатели свидетельствуют о неадекватном потреблении кислорода тканями вследствие выраженных ишемических повреждений. Летальность в этой группе больных достоверно выше.
Но и нормальные или даже повышенные значения VO2 - еще не свидетельство достаточного обеспечения тканей кислородом, поскольку интенсивность метаболизма при критических состояниях может значительно возрастать (например при сепсисе). Поэтому необходимо иметь представление об интенсивности анаэробного метаболизма,
который будет тем выше, чем выраженнее ишемия. Для этих целей используют показатель содержания сывороточного лактата. Концентрация лактата свыше 4 мэкв/л является достоверным признаком выраженной тканевой ишемии [3].
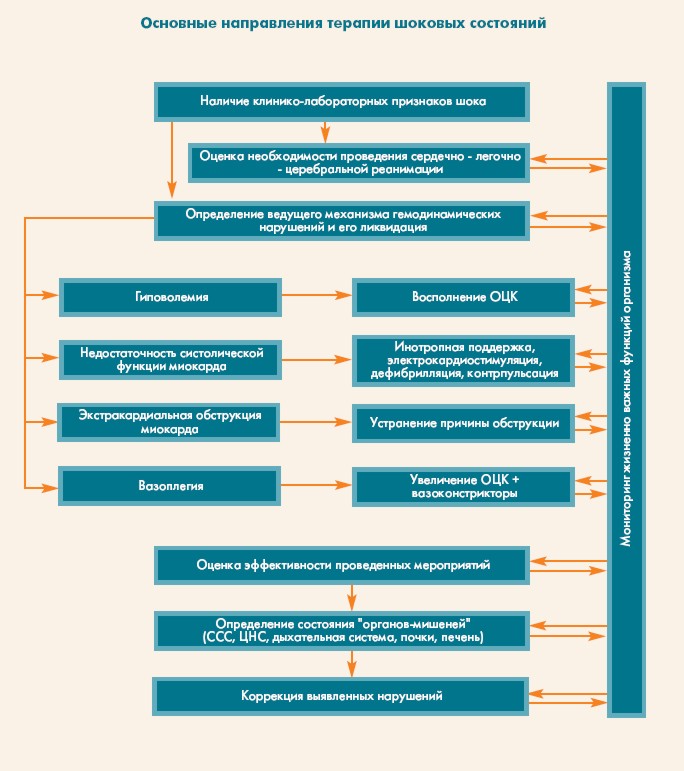
К сожалению, лечение шоковых состояний невозможно полностью изложить в рамках одной статьи. Терапия шока изначально должна быть направлена на устранение ведущего механизма его развития (схема). Поскольку при шоке, как и при любом критическом состоянии, поражаются практически все органы и системы, необходима
ранняя оценка состояния основных из них и своевременная коррекция выявленных нарушений. В конечном счете, главная задача терапии шокового состояния (помимо ликвидации основного заболевания) состоит в восстановлении адекватной микроциркуляции в периферических тканях и кислородного транспорта к ним.
В заключение необходимо сказать, что успех лечения шока во многом зависит от понимания врачом механизма его развития, хотя в целом мировая статистика говорит о достаточно высокой летальности при шоковых
состояниях. Тем не менее знание особенностей каждого из них позволяет врачу не принимать необдуманных решений и тем самым оставить больному больше шансов на выздоровление.
Список литературы
1) Амосова Е.Н. Клиническая кардиология. В двух томах. Т.1. Київ: Книга - плюс, (1998).
2) Зильбер А.П. Клиническая физиология в анестезиологии и реаниматологии. М.: Медицина,(1984).
3) Интенсивная терапия. пер. с англ. (под ред. П. Марино). Издательство "ГЭОТАР Медицина", (1998)
4) Зильбер А.П., Шифман Е.М. Акушерство глазами анестезиолога. "Этюды критической медицины", Т.3. - Петрозаводск: Издательство ПГУ, (1997).
5) Сиренко Ю.И. Кардиогенный шок при инфаркте миокарда: новые возможности терапии.//Український кардіологічний журнал, №4,(1995).
Medicus Amicus 2003, #4
|
|









 Пожилой возраст является фактором риска при раке молочной железы (РМЖ). Большая часть смертей от РМЖ происходит именно у пожилых. Не всегда у них удается провести лечение сог..
Пожилой возраст является фактором риска при раке молочной железы (РМЖ). Большая часть смертей от РМЖ происходит именно у пожилых. Не всегда у них удается провести лечение сог.. включала всех живорожденных детей, а также случаи мертворождения и прерывания беременности вследствие врожденных пороков в 7 канадских провинциях за период 1993 по 2002 гг. Основн..
включала всех живорожденных детей, а также случаи мертворождения и прерывания беременности вследствие врожденных пороков в 7 канадских провинциях за период 1993 по 2002 гг. Основн.. Роль антитромботической терапии при хронической сердечной недостаточности (ХСН) у пациентов с синусовым ритмом обсуждается много лет. В частности, оживленные дискуссии вызывает воп..
Роль антитромботической терапии при хронической сердечной недостаточности (ХСН) у пациентов с синусовым ритмом обсуждается много лет. В частности, оживленные дискуссии вызывает воп.. Жаропонижающие лекарственные средства - препараты, наиболее часто используемые для лечения детей как педиатрами, так и родителями. Этому способствуют бытующие представления об опас..
Жаропонижающие лекарственные средства - препараты, наиболее часто используемые для лечения детей как педиатрами, так и родителями. Этому способствуют бытующие представления об опас.. Неонатальный сепсис (НС) остается ведущей причиной смерти у недоношенных новорождённых. Стратегии для уменьшения частоты НС по-прежнему не достаточно эффективны, и связанная с НС с..
Неонатальный сепсис (НС) остается ведущей причиной смерти у недоношенных новорождённых. Стратегии для уменьшения частоты НС по-прежнему не достаточно эффективны, и связанная с НС с..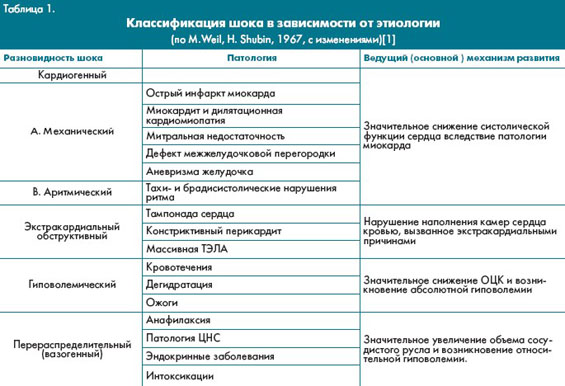


 Новости
Новости 