Исследователи представили способ снизить цены на вакцины
Используя вакцину Зика в качестве модели, исследовательская группа показала, что платформа ДНК эффективно работает на мышах. После однократной низкой дозы вакцина ДНК защ..
| Биологи: люди с повышенной сонливостью в три раза чаще подвержены болезни Альцгеймера
Ученые из Университета Джона Хопкинса в США под руководством биолога Адама Спира выявили, что люди с повышенной дневной сонливостью в три раза чаще страдают от&..
| Биологи обнаружили три неуязвимых для антибиотиков бактерии
Каждый год только в США по меньшей мере 2 млн человек заражаются супербактериями — штаммами, устойчивыми к существующим антибиотикам. Из-за отсутстви..
| Новый анализ крови предсказывает рак почек задолго до диагноза
В новом исследовании, опубликованном в журнале Clinical Cancer Research, ученые вместе с коллегами из Израильского диагностического центра задались вопросом: мо..
| Новый наноматериал уничтожит пленки из микробов, которые развивают кариес
Американские химики представили наноматериал, растворяющий пленки из микробов, которые формируют налет и развивают кариес...
| Українцям робитимуть щеплення за новим графіком
Як пояснили в Міністерстві охорони здоров’я, оновлення в календарі стосуються вакцинації проти гепатиту В та туберкульозу. ..
| Смертельный вирус угрожает пандемией
Число жертв вируса Нипах, эпидемия которого началась на юге Индии, уже достигло семнадцати человек. По словам медиков, на данный момент нет ни вакцины, ни лечения вызываемого вирус..
|
| Принципы патогенетической терапии бронхиальной астмы у детей раннего возраста
лечение бронхиальной астмы у детей раннего возраста лечение бронхиальной астмы острый бронхоспазм отек слизистой оболочки бронхов гиперсекреция слизи ремоделирование стенки бронхов степени тяжести бронхиальной астмы ГКС b2-агонисты метилксантины
Принципы патогенетической терапии бронхиальной астмы у детей раннего возраста
Охотникова Е.Н., доктор медицинских наук, доцент кафедры педиатрии №1, Киевская медицинская академия последипломного образования им. П.Л. Шулика
Последнее десятилетие ознаменовалось пересмотром взглядов на патогенез бронхиальной астмы (БА) как у взрослых, так и у детей. Доказано, что в основе заболевания лежит хронический воспалительный процесс
дыхательных путей, который обуславливает их гиперреактивность, что клинически проявляется бронхообструктивным синдромом и другими респираторными симптомами [1].
Основой воспаления при БА является повышенная активность эозинофилов, мастоцитов, макрофагов, Т2-лимфоцитов-хелперов, эпителиоцитов, эндотелиальных клеток гладкой мускулатуры бронхов с последующей секрецией и активацией цитокинов и других медиаторов, способствующих хронизации воспаления [2].
В результате воспалительного процесса формируются 4 варианта бронхиальной обструкции:
- острый бронхоспазм;
- отек слизистой оболочки бронхов;
- гиперсекреция слизи и обусловленная этим обтурация мокротой просвета бронхов;
- ремоделирование стенки бронхов (структурные изменения в бронхах различного калибра).
Учитывая морфофункциональные особенности органов дыхания у детей раннего возраста
(узость дыхательных путей, недостаточная эластичность легких, податливость хрящей бронхов, недостаточная ригидность грудной клетки, слабое развитие гладкой мускулатуры бронхов, обильная васкуляризация дыхательных путей, гиперсекреция бокаловидными клетками вязкой слизи), ведущими компонентами бронхообструкции у больных первых лет жизни
являются выраженный отек слизистой бронхов и гиперсекреция слизи [3]. Эти анатомо-физиологические особенности необходимо учитывать в терапии БА у детей младшего возраста при составлении индивидуального плана лечебных мероприятий, поскольку
БА очень часто протекает тяжело, нередко со слабой эффективностью бронхолитической терапии во время лечения острых эпизодов заболевания [4].
Исходя из воспалительной концепции развития болезни, ключевыми положениями терапии БА у детей раннего возраста являются:
- Лечение назначается с учетом степени тяжести и периода болезни у
конкретного больного, доступности противоастматических препаратов и индивидуальных, социальных, семейных и экономических особенностей семьи больного ребенка.
- Терапия БА состоит из комплекса мероприятий во время обострения и в период ремиссии.
- Наиболее эффективными препаратами для контроля БА являются ингаляционные глюкокортикостероиды (ИГКС). Длительная терапия ИГКС резко снижает частоту и тяжесть обострений.
- Наиболее эффективными симптоматическими препаратами при лечении обострений БА являются ингаляционные b2-агонисты быстрого действия, которые являются также самыми эффективными среди существующих бронхолитиков.
- После достижения ремиссии при сохранении контроля за течением БА в течение не менее 3 месяцев доза поддерживающей терапии может быть постепенно уменьшена до минимально необходимой.
- Многие препараты (ГКС, b2-агонисты, метилксантины) у детей младшего возраста метаболизируются быстрее, чем у детей старшего возраста и взрослых, в связи с чем при пероральном назначении препарат должен применяться в более высоких дозах, чем у старших детей.
- Длительная терапия ИГКС не приводит к увеличению остеопороза и переломов костей, не влияет на рост ребенка.
Течение БА можно считать контролируемым, если:
- признаки болезни, включая ночные симптомы, минимально выражены (в идеале - отсутствуют);
- обострения заболевания эпизодические;
- отсутствует необходимость в применении средств неотложной помощи (b2-агониста) или потребность в них очень низкая;
- отсутствует необходимость в ограничении активности ребенка, особенно физической;
- побочные эффекты от применения длительной фармакотерапии слабо выражены или отсутствуют.
Лекарственные препараты для лечения БА у детей делятся на две основные группы:
- Средства для контроля за течением болезни, направленные на постоянное подавление хронического аллергического воспаления в дыхательных путях (противовоспалительная базисная фармакотерапия), которые принимаются ежедневно и длительно.
- Средства для неотложной помощи, которые действуют быстро, купируя бронхоконстрикцию и сопутствующие ей признаки обострения, (свистящее дыхание с затрудненным выдохом, слышимое на расстоянии, кашель) и которые используются только для лечения обострений БА.
Преимущественным путем введения препаратов является ингаляционный, поскольку он позволяет создать высокие и эффективные концентрации медикаментов непосредственно в дыхательных путях и свести к минимуму развитие системных побочных
действий. Введение препаратов производится с помощью различных средств ингаляционной техники (доставочных устройств). Поскольку маленькие дети (включая больных грудного возраста) не могут активно координировать дыхательные движения, для
осуществления контролирующей (противовоспалительной) терапии лучше использовать дозированный аэрозольный ингалятор (ДАИ) в комбинации с задерживающей камерой (бебихалером, спейсером, синхронером, аутохалером).
Для оказания неотложной помощи и интенсивной терапии с использованием бронхолитиков применяются ДАИ в сочетании со спейсером и лицевой маской или ингаляции проводятся через небулайзер. За неимением устройств
фабричного производства альтернативой может быть самодельное приспособление из пластиковой бутылки, у которой отрезается дно, а горлышко с помощью горячей воды моделируется под размер мундштука дозированного ингалятора.
Противовоспалительная терапия назначается непрерывным курсом общей продолжительностью не менее 6 месяцев (из них 3 месяца - в оптимальной дозе и 3 месяца - постепенное снижение до минимальной дозы, поддерживающей контроль БА). Это минимальный срок, необходимый для подавления аллергического воспаления в дыхательных путях.
В качестве базисной терапии используются различные ИГКС (беклометазона дипропионат, флютиказона пропионат, будесонид), ингаляционные нестероидные противовоспалительные препараты (кромоны, недокромил натрия) и антилейкотриены (монтелукаст,
зафирлукаст).
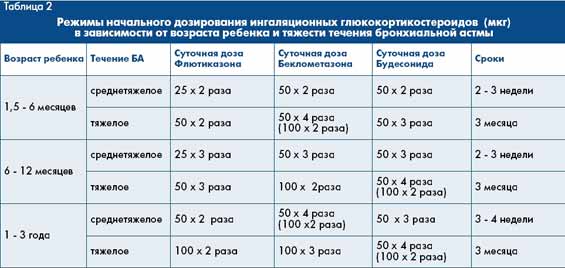
При назначении противовоспалительной терапии используют ступенчатый подход (таблицa 1), который предусматривает различный объем и интенсивность медикаментозного лечения в зависимости от степени тяжести течения (выраженности симптомов) [5].
Принцип ступенчатого подхода к проведению противовоспалительной терапии предусматривает 2 методики назначения препаратов - "ступенька вверх" и "ступенька вниз". У детей раннего возраста при первых эпизодах болезни, когда еще неизвестен дальнейший характер течения БА, чаще используется методика "ступенька вверх".
При этом назначается такой вариант лечения, который соответствует степени тяжести заболевания непосредственно перед началом лечения.
В случае отсутствия эффекта от проводимого на протяжении 2-3 недель лечения или утяжеления дальнейшего течения болезни необходимо увеличить дозу противовоспалительного препарата или поменять его на более мощный (кромоны
- на ИГКС). Методика "ступенька вниз" предполагает сразу назначение более интенсивных медикаментов для достижения быстрого эффекта с постепенным снижением дозы и в период устойчивой ремиссии сменой препарата на более щадящий
(ИГКС - на кромоны). Такой подход является более целесообразным при тяжелом дебюте БА у больных младшего возраста, особенно у детей со значительно отягощенной по атопии семейной наследственностью, у которых прогноз дальнейшего
течения процесса более серьезен. В связи с тем, что в этом возрасте БА протекает у большинства больных тяжело [2, 4], на начальном этапе лечения предпочтительна методика "ступенька вниз".
Согласно современным рекомендациям [1,2], наиболее эффективными базисными препаратами у детей раннего возраста являются ИГКС, терапия которыми должна проводиться с первых дней острого периода болезни
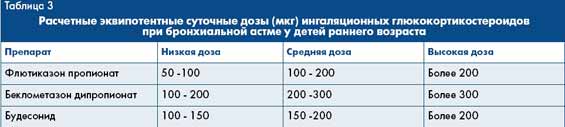
при среднетяжелом и тяжелом течении заболевания. Это предотвращает возможность последующих рецидивов БА. Начальные дозы ИГКС для больных первых лет жизни [6] даны в таблице 2, а эквипотентные суточные дозировки - в таблице 3.
Назначение ИГКС позволяет значительно уменьшить использование системных парентеральных и, тем более, пероральных ГКС. Пробную терапию ИГКС коротким курсом нужно шире применять в лечении рецидивирующего бронхообструктивного синдрома у детей первых лет жизни с ранними проявлениями аллергии, поскольку влияние ИГКС на хроническое
воспаление предупреждает формирование персистирующей БА и инвалидизацию больного. Применение низких и среднетерапевтических доз ИГКС позволяет эффективно и безопасно контролировать болезнь у подавляющего большинства детей с тяжелым течением.
При назначении высоких доз ИГКС обязательно следует учитывать соотношение между пользой и потенциальной опасностью лечения ими. Наиболее значимым, но редким (менее 1%) возможным побочным эффектом длительной терапии
ИГКС является кандидоз слизистой полости рта. Для его профилактики рекомендуется через 15-20 минут после ингаляции предложить ребенку выпить немного воды.
С целью уменьшения дозы ИГКС при тяжелом течении можно сочетать их с пролонгированными b2-агонистами (25 мкг сальметерола в 1 вдохе). Последние обладают и бронходилатирующим эффектом в течение 12 часов,
и некоторым противовоспалительным действием. Их можно назначать одновременно и с негормональными препаратами для усиления терапии ингаляционными противовоспалительными препаратами (ИНПВП) перед принятием решения о назначении ИГКС.
ИНПВП применяются у детей с легким течением БА и у части больных со среднетяжелым вариантом болезни, у которых астма протекает в виде периодических обострений, а персистирующие симптомы слабо выражены.
ИНПВП следует использовать в адекватных дозах в течение всего периода лечения. У больных со среднетяжелым течением в период сезонных обострений хороший профилактический эффект достигается дополнительным назначением короткого курса (4-6 недель) ИГКС в низких дозах на фоне длительной терапии ИНПВП, что обеспечивает удовлетворительный
контроль за течением БА у большинства детей. Правильное распределение противовоспалительной терапии позволяет проводить плановый перерыв в лечении в наиболее благоприятный для больного период.
Антилейкотриеновые препараты (чаще монтелукаст, который назначается детям с двухлетнего возраста) показаны больным с астмой физического и психоэмоционального напряжения и особенно детям, у которых были проблемы
с использованием ингаляционной техники, поскольку, в отличие от ингаляционных средств, применяются в пероральной форме. При необходимости их можно комбинировать с ИНПВП и ИГКС с целью уменьшения их общей дозы.
Метилксантины у детей младшего возраста должны использоваться в лечении обострений как терапия "отчаяния", если предпринятое лечение с использованием b2-агонистов быстрого действия, холинолитиков,
парентеральных и ингаляционных ГКС не эффективно. Для длительной базисной терапии у детей раннего возраста они не должны применяться в связи с большой опасностью развития серьезных побочных реакций.
Использование в лечении острых эпизодов БА у детей первых лет жизни ингаляционных холинолитиков патогенетически оправдано и высоко эффективно, что объясняется преобладанием у них ваготонии. Их
хорошо применять в начале обострения болезни, но не долго и в комбинации с муколитиками, вводимыми при тяжелом приступе внутривенно. Это обусловлено подсушивающим эффектом производных атропина. Более выраженное бронхолитическое действие
отмечается при сочетании окситропиума бромида и b2-агонистов быстрого действия, поскольку они потенцируют активность друг друга.
При их неэффективности возможно применение b2-агонистов быстрого действия перорально и парентерально.
В формировании БА у детей младшего возраста большую роль играют возбудители респираторных
инфекций - вирусы и бактерии, в том числе атипичные [7]. В связи с этим во время обострений астмы часто нужно решать вопрос о назначении антибиотиков, а в период ремиссии - иммуностимуляторов микробного происхождения.
Показаниями для назначения антибиотиков при БА являются:
- затяжной астматический приступ;
- астматический статус;
- инфицирование больного патогенными и атипичными микробами (гемофильной палочкой, микоплазмами, хламидиями, золотистым стафилококком, стрептококком пневмонии и др.);
- хронические очаги инфекции;
- вторичный катарально-гнойный и гнойный эндобронхит.
Выбор антибактериального препарата довольно ограничен: цефалоспорины, фторхинолоны, макролиды. Преимущество следует отдавать макролидам последнего поколения (азитромицину, кларитромицину, спирамицину), которые
имеют высокую эффективность в отношении указанных бактериальных возбудителей, создают высокую концентрацию в очаге воспаления при пероральном введении, практичеки не имеют побочных эффектов, удобны в применении, хорошо воспринимаются маленькими детьми.
Показания для назначения бактериальных иммуностимуляторов:
- отягощенный инфекционный анамнез у ребенка;
- сопутствующие очаги инфекций;
- ОРЗ в качестве триггера (провокатора) БА;
- инфекционный синдром при обострении БА;
- лабораторно подтвержденное снижение показателей иммунного статуса (клеточного и гуморального звеньев иммунитета, факторов местной защиты и фагоцитоза);
- обнаружение возбудителей (в смывах слизи из носа, зева, в мокроте).
Лечение БА у детей раннего возраста не должно быть агрессивным. Следует стремиться к достижению контроля за течением болезни наиболее эффективными и более безопасными базисными средствами, избегать одновременного назначения большого количества препаратов. Идеальным вариантом является монотерапия. Благодаря ранней диагностике
и своевременно начатой базисной терапии БА, прежде всего у детей раннего возраста, за последнее десятилетие в Украине практически полностью ликвидирована так называемая гормонозависимость: резко сократилось (до единичных случаев) число детей, требующих длительного использования системных ГКС. Взвешенная тактика базисного лечения БА позволяет
значительно улучшить качество жизни, физическое развитие больных, ликвидировать тяжелые побочные эффекты системной гормонотерапии.
Литература
1. Глобальная стратегия лечения и профилактики бронхиальной астмы (Global Initiative For Asthma). Москва, Атмосфера (2002).
2. Ласица О.И., Ласица Т.С. Бронхиальная астма в практике семейного врача. Киев, ЗАО "Атлант UMS" (2001).
3. Стефани Д.В., Вельтищев Ю.Е. Иммунология и иммунопатология детского возраста (руководство для врачей). Москва, Медицина (1996).
4. Охотнікова О.М. Особливості бронхіальної астми у дітей перших років життя. Педіатрія, акушерство і гінекологія, №4 (1999).
5. Ласиця О.Л., Охотнікова О.М. Бронхіальна астма у дітей: проблеми і перспективи діагностики і лікування. Нова медицина, №1(6) (2003).
6. Охотнікова О.М. Особливості патогенетичної терапiї бронхіальної астми у дітей першого року життя. Збірник наук. праць співроб. КМАПО ім. П.Л.Шупика, присвяч. 85-річному ювілею. Київ, кн. 2 (2003).
7. Кузьменко Л.Г. Значение внутриклеточных патогенов в формировании хронических бронхолегочных заболеваний. Детские инфекции, №1 (2003).
Medicus Amicus 2004, #3
|
|















 Новости
Новости 