Остеоартроз
Остеоартроз (ОА) – хроническое прогрессирующее дегенеративное заболевание суставов, характеризующееся деградацией суставного хряща с последующими изменениями в субхондральной кости и формированием остеофитов, приводящее к потере
хрящевой ткани с частичной или даже полной утратой функции суставов. Чаще всего поражаются крупные нагрузочные суставы (коленные, тазобедренные), позвоночник и мелкие суставы кисти. В западной литературе ОА носит название «остеоартрит», что отражает его воспалительную природу.
Распространенность
ОА является самой распространенной формой патологии суставов. Только в США им страдают более 20 миллионов человек. Рентгенологические признаки ОА коленных суставов обнаруживаются у 30% лиц обоего пола в возрасте старше
50 лет, при этом у 10 % из них имеют место клинические симптомы. По данным ВОЗ, артроз коленного сустава (гонартроз) занимает 4-е место среди причин
нетрудоспособности у женщин и 8-е – у мужчин. Частота ОА увеличивается с возрастом. Мужчин ОА чаще поражает после 45 лет, женщин – после 55. ОА - одна из основных причин инвалидизации и хронического болевого синдрома, значительно снижающего качество жизни пациентов.
Этиология и патогенез
В большинстве случаев причина ОА остается неустановленной. Основные факторы риска: пожилой возраст, женский пол, генетическая предрасположенность, избыточная масса тела, травмы и оперативные вмешательства на суставах, снижение уровня женских половых гормонов в период менопаузы, избыточные нагрузки на сустав.
В физиологических условиях для адаптации к механическим нагрузкам
хрящевая ткань постоянно обновляется, что осуществляется посредством пролиферации хондроцитов и усиления синтеза ими компонентов межклеточного матрикса. При длительных нагрузках на сустав и воздействии факторов риска процессы обновления хрящевой ткани нарушаются и дегенеративные процессы начинают
преобладать над восстановительными. В результате происходит истончение и потеря гидрофильности суставного хряща, в нем образуются трещины и очаги обызвествления.
Важную роль в процессе дегенерации хряща играют провоспалительные
цитокины, стимулирующие катаболизм соединительнотканного матрикса и подавляющие синтез коллагена и протеогликанов. В ответ на дегенеративно-воспалительные процессы в хряще происходят изменения в субхондральной кости: склероз, микропереломы, формирование кист, разрастание остеофитов.
Фрагменты разрушенного хряща, попадая в полость сустава, подвергаются фагоцитозу с выделением медиаторов воспаления, способствуя распространению воспалительного процесса на синовиальную оболочку, капсулу сустава и дальнейшему прогрессированию дегенерации хряща.
Клиническое течение
Характеризуется волнообразностью со сменой коротких периодов обострения спонтанной ремиссией. Основными жалобами являются боль, скованность, уменьшение объема движений в суставах (тугоподвижность). Боль носит
«механический» характер – появляется при физической нагрузке и уменьшается в покое. Характерны вечерние и ночные боли после дневной нагрузки. На поздних стадиях при полной потере хрящевой прокладки боли могут беспокоить и в покое. Возможна кратковременная «стартовая» боль после периода покоя, проходящая на
фоне двигательной активности. Она возникает при трении суставных поверхностей, на которых оседает хрящевой детрит. При первых движениях в суставе детрит выталкивается в суставную полость и боль значительно уменьшается или прекращается полностью. При ущемлении костного или хрящевого
отломка («суставной мыши») между суставными поверхностями возникает резкая боль, которая делает невозможыми движения в суставе («блокада сустава»). После выскальзывания отломка боль прекращается.
Кроме болевого синдрома может беспокоить скованность в суставах длительностью до
15 - 30 минут после отдыха или ночного сна. Движения в пораженном суставе ограничены вследствие болевого синдрома, а на более поздних стадиях – за счет деформации сустава, образования сухожильно-мышечных контрактур.
При пальпации суставов может определяться крепитация, которая при прогрессировании
заболевания может переходить в грубый хруст при движениях.
Специфичным для ОА является появление плотных узелков в области дистальных (Гебердена) и проксимальных (Бушара) межфаланговых суставов. Пальпация их часто болезненна, они могут ограничивать движения в суставах.
Появление локальных изменений (припухлость в области сустава с гиперемией и повышением температуры кожных покровов, болезненность при пальпации) свидетельствует о реактивном синовите.
Диагностические критерии
Диагностика в большинстве случаев не представляет значительных
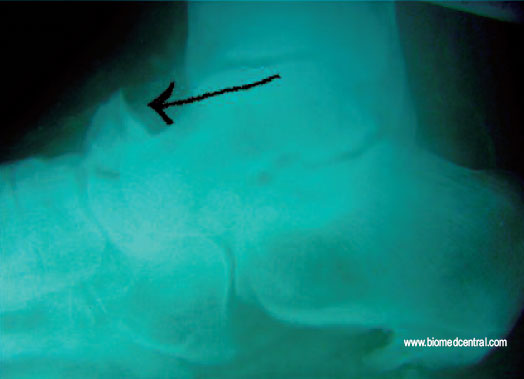
трудностей. Наиболее распространенным методом остается рентгенологическое исследование, которое также помогает установить стадию заболевания. В пользу ОА свидетельствуют сужение суставной щели, субхондральный склероз, остеофиты, субхондральные кисты.
Довольно распространенным методом диагностики является
артроцентез, позволяющий провести исследование суставной жидкости для исключения подагры, инфекции и других причин. Типичная для артроза синовиальная жидкость –00 светлая, вязкая с числом лейкоцитов менее 2000/мл.
Артроскопия является хирургической процедурой, в ходе которой
в суставную щель вводится визуализирующий прибор. При этом могут быть выявлены, а иногда и восстановлены аномалии и повреждения хряща и связок. После успешной артроскопии пациенты восстанавливаются гораздо быстрее, чем после открытых хирургических вмешательств на суставах.
При необходимости используют УЗИ, сцинтиграфию, компьютерную или магниторезонансную томографию.
Общепринятые исследования крови не имеют диагностического значения. В период обострения с развитием синовита возможно ускорение СОЭ и повышение острофазовых белков.
Лечение
Основной целью лечения является уменьшение выраженности болевого синдрома и степени функциональной недостаточности сустава, предотвращение или замедление прогрессирования заболевания и развития
осложнений.
Немедикаментозные методы включают информирование пациента о заболевании (обучающие программы), изменение образа жизни, уменьшение массы тела, регулярные физические упражнения, уменьшение
механической нагрузки на сустав (ортопедические стельки, трости, шины, фиксация коленного сустава), физиотерапевтические процедуры. У некоторых больных консервативные методы дают высокую эффективность. Имеются данные, что даже незначительное уменьшение массы тела способно ослабить
симптомы ОА коленных и тазобедренных суставов.
В медикаментозном лечении используются ацетаминофен, нестероидные противовоспалительные препараты (НПВП), опиоидные анальгетики и кортикостероиды (оказывают влияние на клинические
проявления заболевания – боль и воспаление), а также препараты глюкозамина и хондроитина сульфата, диацереин, неомыляющиеся компоненты авокадо и соевых бобов, экстракт имбиря, обладающие хондромодифицирующим действием и предупреждающие деградацию суставного хряща.
В соответствии с рекомендациями специалистов по ведению пациентов с ОА коленных и тазобедренных суставов в качестве стартовой, а при положительном эффекте и длительной терапии используется парацетамол в дозе 2,5-4 г в сутки. У многих пациентов его действие при кратковременном использовании сравнимо с ибупрофеном и напроксеном. При этом он имеет лучший
профиль безопасности по сравнению с неселективными НПВП.
При неэффективности парацетамола через 7-10 дней от начала лечения, а также синовите показаны НПВП (самостоятельно или в комбинации с парацетамолом). У пациентов с повышенным риском желудочно-кишечных заболеваний
используются неселективные НПВП в комбинации с гастропротекторами (ингибиторы протонной помпы, блокаторы Н2-рецепторов, мизопростол) или селективные и специфические ингибиторы ЦОГ-2 . Особый интерес вызывает хондропротективный эффект целекоксиба. Имеются данные, что он положительно влияет на
метаболизм хрящевой ткани, увеличивая синтез протеогликанов и гиалуроновой кислоты.
Эффективны также местные аппликации НПВС, предпочтительнее на гелевой основе.
Опиоидные анальгетики могут применяться при наличии
противопоказаний к НПВП и в случае их неэффективности и/или плохой переносимости.
Внутрисуставные инъекции глюкокортикоидов продленного действия показаны при выраженном болевом синдроме, особенно при наличии суставного выпота.
Из хондропротекторных препаратов только глюкозамина и хондроитина сульфат имеют высокий уровень доказательности. Препараты обладают высокой биодоступностью и хорошей переносимостью.
Грубые нарушения структуры и функции тазобедренных и коленных суставов в сочетании с рефрактерным болевым синдромом являются показанием для эндопротезирования. Артропластика является эффективным методом лечения, существенно улучшающим качество жизни пациентов.
Подготовила И. Бурда
Рекомендуемые источники
http://ard.bmj.com/
http://www.eular.org/
www.arthritis.org
Medicus Amicus
|














 Новости
Новости 